Cuantos Tipos De Vitamina D Hay
El enlace químico es la fuerza que logra mantener unidos los átomos que componen la materia. Cada tipo de materia posee un enlace químico característico, el cual consiste en la participación de uno o más electrones. Así, las fuerzas que unen los átomos en los gases son diferentes, por ejemplo, a la de los metales.
Todos los elementos de la tabla periódica (a excepción del helio y los gases nobles livianos) pueden formar enlaces químicos unos con otros. Sin embargo, la naturaleza de éstos se modifica dependiendo de qué elementos provienen los electrones que los forman. Un parámetro esencial para explicar el tipo de enlaces es la electronegatividad.
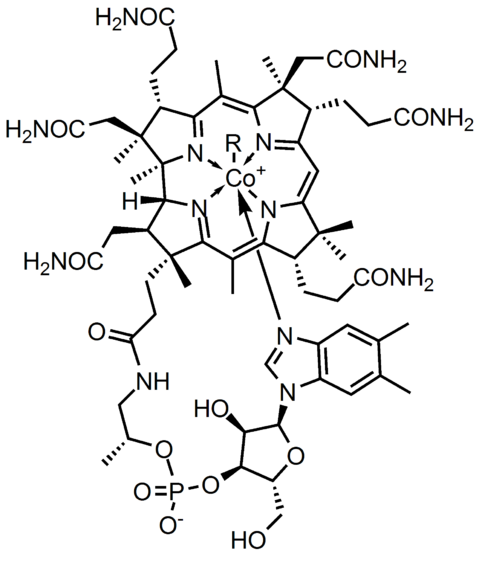
La diferencia de electronegatividad (ΔE) entre dos átomos define no sólo el tipo de enlace químico, sino además, las propiedades fisicoquímicas del compuesto. Las sales se caracterizan por tener enlaces iónicos (ΔE alto), y muchos de los compuestos orgánicos, como la vitamina B12 (imagen superior), enlaces covalentes (ΔE bajo).
En la estructura molecular superior, cada una de las líneas representa un enlace covalente. Las cuñas indican que el enlace emerge del plano (hacia el lector), y las subrayadas detrás del plano (alejándose del lector). Nótese que hay dobles enlaces (=) y un átomo de cobalto coordinado con cinco átomos de nitrógeno y una cadena lateral R.
Pero, ¿por qué se forman tales enlaces químicos? La respuesta se encuentra en la estabilidad energética de los átomos y electrones participantes. Esta estabilidad debe equilibrar las repulsiones electrostáticas experimentadas entre las nubes electrónicas y los núcleos, y la atracción ejercida por un núcleo sobre los electrones del átomo vecino.
Índice del artículo
- 1 Definición del enlace químico
- 2 Características
- 3 ¿Cómo se forman los enlaces químicos?
- 3.1 Compuestos homonucleares A-A
- 3.2 Compuestos heteronucleares A-B
- 4 Tipos de enlaces químicos
- 4.1 -Enlace covalente
- 4.2 -Enlace iónico
- 4.3 Enlace metálico
- 5 Ejemplos de enlaces
- 6 Importancia del enlace químico
- 7 Referencias
Definición del enlace químico
Muchos autores han dado definiciones del enlace químico. De todas ellas la más importante fue la del fisicoquímico G. N. Lewis, quien definió el enlace químico como la participación de un par de electrones entre dos átomos. Si los átomos A· y ·B pueden aportar un solo electrón, entonces se formará entre ellos el enlace sencillo A:B o A–B.
Antes de la formación del enlace, tanto A como B están separados por una distancia indefinida, pero al enlazarse existe ahora una fuerza que los mantiene unidos en el compuesto diatómico AB y una distancia (o longitud) de enlace.
Características

¿Qué características posee esta fuerza que mantiene unido los átomos? Estas dependen más del tipo de enlace entre A y B que de sus estructuras electrónicas. Por ejemplo, el enlace A–B es direccional. ¿Qué quiere decir? Que la fuerza ejercida por la unión del par de electrones puede representarse en un eje (como si fuera un cilindro).
Asimismo, este enlace requiere de energía para romperse. Esta cantidad de energía puede venir expresada en las unidades de kJ/mol o cal/mol. Una vez aplicada la suficiente energía sobre el compuesto AB (mediante calor, por ejemplo), este se disociará en los átomos A· y ·B originales.
Mientras más estable sea el enlace, mayor es la cantidad de energía que requiere para separar los átomos unidos.
Por otro lado, si el enlace en el compuesto AB fuera iónico, A+B–, entonces se trataría de una fuerza no direccional. ¿Por qué? Porque A+ ejerce una fuerza de atracción sobre B– (y viceversa) que depende más de la distancia que separa ambos iones en el espacio que de una ubicación relativa de los mismos.
Este campo de atracción y repulsión reúne a otros iones para formar lo que se conoce como red cristalina (imagen superior: el catión A+ yace rodeado de cuatro aniones B–, y estos de cuatro cationes A+ y así sucesivamente).
¿Cómo se forman los enlaces químicos?
Compuestos homonucleares A-A

Para que un par de electrones formen un enlace hay muchos aspectos que deben considerarse primero. Los núcleos, a decir los de A, tienen protones y son por lo tanto positivos. Cuando dos átomos de A se encuentran muy alejados entre sí, es decir, a una distancia internuclear grande (imagen superior), estos no experimentan ninguna atracción.
A medida que se aproximan los dos átomos de A sus núcleos atraen la nube electrónica del átomo vecino (el círculo morado). Esta es la fuerza de atracción (A sobre el círculo morado vecino). Sin embargo, los dos núcleos de A se repelen por ser positivos, y esta fuerza aumenta la energía potencial del enlace (eje vertical).
Existe una distancia internuclear en la cual la energía potencial alcanza un mínimo; es decir, se equilibran tanto la fuerza de atracción como la de repulsión (los dos átomos de A en la parte inferior de la imagen).
Si esta distancia disminuye después de este punto, el enlace ocasionará que los dos núcleos se repelan con mucha fuerza, desestabilizando el compuesto A-A.
Entonces, para que el enlace se forme debe haber una distancia internuclear energéticamente adecuada; y además, los orbitales atómicos deben traslaparse correctamente para que los electrones se enlacen.
Compuestos heteronucleares A-B
¿Y si en lugar de dos átomos de A se unieran uno de A y otro de B? En dicho caso la gráfica superior cambiaría porque uno de los átomos tendría más protones que el otro, y las nubes electrónicas diferentes tamaños.
Al formarse el enlace A–B a la adecuada distancia internuclear, el par de electrones se encontrará principalmente en las cercanías del átomo más electronegativo. Esto sucede así con todos los compuestos químicos heteronucleares, los cuales constituyen la inmensa mayoría de los que se conocen (y se conocerán).
Aunque no se mencionen con profundidad, hay numerosas variables que influyen directamente en cómo se aproximan los átomos y se forman los enlaces químicos; algunas son termodinámicas (¿es espontánea la reacción?), electrónicas (qué tan llenos o vacíos están los orbitales de los átomos) y otras cinéticas.
Tipos de enlaces químicos
Los enlaces presentan una serie de características que los distinguen unos de otros. Varias de ellas pueden enmarcarse en tres principales clasificaciones: covalentes, iónicos o metálicos.
Aunque hay compuestos cuyos enlaces pertenecen a un único tipo, muchos en realidad consisten de una mezcla de caracteres de cada uno. Este hecho se debe a la diferencia de electronegatividad entre los átomos que forman los enlaces. Así, algunos compuestos pueden ser covalentes, pero presentan en sus enlaces cierto carácter iónico.
Asimismo, el tipo de enlace, la estructura y la masa molecular, son factores claves que definen las propiedades macroscópicas de la materia (brillo, dureza, solubilidad, punto de fusión, etc.).
-Enlace covalente
Los enlaces covalentes son aquellos que han venido explicándose hasta el momento. En ellos, dos orbitales (un electrón en cada uno) deben traslaparse con los núcleos separados a una apropiada distancia internuclear.
De acuerdo a la teoría del orbital molecular (TOM), si el traslape de los orbitales es frontal se formará un enlace sigma σ (al cual también se le llama enlace sencillo o simple). Mientras que si los orbitales se forman por traslapes laterales y perpendiculares respecto al eje internuclear, se tendrán los enlaces π (doble y triple):

Enlace sencillo
El enlace σ como puede apreciarse en la imagen se forma a lo largo del eje internuclear. A pesar de que no se muestre, A y B pueden tener otros enlaces, y por lo tanto, sus propios entornos químicos (distintas partes de la estructura molecular). Este tipo de enlace se caracteriza por su poder de rotación (cilindro verde) y por ser el más fuerte de todos.
Por ejemplo, el enlace sencillo de la molécula de hidrógeno puede rotar sobre el eje internuclear (H–H). Del mismo modo, puede hacerlo una molécula hipotética CA–AB.
Los enlaces C–A, A–A y A–B rotan; pero si C o B son átomos o un grupo de átomos voluminosos, la rotación A–A se ve impedida estéricamente (porque chocarían C y B).
Los enlaces sencillos se encuentran prácticamente en todas las moléculas. Sus átomos pueden tener cualquier hibridación química siempre y cuando el traslape de sus orbitales sea frontal. Volviendo a la estructura de la vitamina B12, cualquiera línea sola (–) indica un enlace sencillo (por ejemplo, los enlaces –CONH2).
Enlace doble
El enlace doble requiere que los átomos posean (de ordinario) hibridación sp2. El enlace p puro, perpendicular a los tres orbitales híbridos sp2, forma el enlace doble, el cual se muestra como una lámina grisácea.
Nótese que tanto el enlace sencillo (cilindro verde) como el doble (lámina grisácea) coexisten al mismo tiempo. Sin embargo, a diferencia de los enlaces sencillos, los dobles no presentan la misma libertad de rotación entorno al eje internuclear. Esto se debe a que, para rotar, el enlace (o la lámina) debe romperse; proceso el cual necesita energía.
Asimismo, el enlace A=B es más reactivo que A–B. La longitud de éste es menor y los átomos A y B se encuentran a una menor distancia internuclear; por lo tanto, hay mayor repulsión entre ambos núcleos. Romper ambos enlaces, el sencillo y el doble, requiere más energía que la que se necesita para separar los átomos en la molécula de A–B.
En la estructura de la vitamina B12 pueden observarse varios enlaces dobles: C=O, P=O, y dentro de los anillos aromáticos.
Enlace triple
El enlace triple es aún más corto que el enlace doble y su rotación se encuentra más impedida energéticamente. En él, se forman dos enlaces π perpendiculares entre sí (las láminas grisácea y morada), así como un enlace sencillo.
De ordinario, la hibridación química de los átomos de A y de B debe ser sp: dos orbitales sp separados 180º, y dos orbitales p puros perpendiculares a los primeros. Nótese que un triple enlace se parece a una paleta, pero sin poder de rotación. Este enlace puede representarse sencillamente como A≡B (N≡N, molécula de nitrógeno N2).
De todos los enlaces covalentes, este es el más reactivo; pero al mismo tiempo, el que necesita de mayor energía para la completa separación de sus átomos (·A: + :B·). Si la vitamina B12 tuviera un enlace triple dentro de su estructura molecular, su efecto farmacológico cambiaría drásticamente.
En los enlaces triples participan seis electrones; en los dobles, cuatro electrones; y en los sencillos o simples, dos.
La formación de uno o más de estos enlaces covalentes depende de la disponibilidad electrónica de los átomos; es decir, de cuántos electrones necesitan sus orbitales para adquirir un octeto de valencia.
Enlace no polar
Un enlace covalente consiste de una compartición equitativa de un par de electrones entre dos átomos. Pero esto es estrictamente cierto solamente en el caso donde ambos átomos tengan iguales electronegatividades; esto es, la misma tendencia de atraer densidad electrónica de su entorno dentro de un compuesto.
Los enlaces no polares se caracterizan por una diferencia de electronegatividad nula (ΔE≈0). Esto ocurre en dos situaciones: en un compuesto homonuclear (A2), o si los entornos químicos a ambos lados del enlace son equivalentes (H3C–CH3, molécula de etano).
Ejemplos de enlaces no polares se ven en los siguientes compuestos:
-Hidrógeno (H–H)
-Oxígeno (O=O)
-Nitrógeno (N≡N)
-Flúor (F–F)
-Cloro (Cl–Cl)
-Acetileno (HC≡CH)
Enlaces polares
Cuando existe una diferencia marcada de electronegatividad ΔE entre ambos átomos, se forma un momento dipolar a lo largo del eje de enlace: Aδ+–Bδ-. En el caso del compuesto heteronuclear AB, B es el átomo más electronegativo, y por tanto, tiene mayor densidad electrónica δ-; mientras que A, el menos electronegativo, deficiencia de carga δ+.
Para que se den los enlaces polares deben unirse dos átomos con diferentes electronegativades; y así, formar compuestos heteronucleares. A–B se asemeja a un imán: tiene un polo positivo y otro negativo. Esto le permite interaccionar con otras moléculas mediante fuerzas dipolo-dipolo, entre las cuales están los puentes de hidrógeno.
El agua tiene dos enlaces covalentes polares, H–O–H, y su geometría molecular es angular, lo cual incrementa su momento dipolar. Si su geometría fuera lineal, los océanos se evaporarían y el agua tendría un punto de ebullición menor.
El hecho de que un compuesto posea enlaces polares, no implica que éste sea polar. Por ejemplo, el tetracloruro de carbono, CCl4, tiene cuatro enlaces polares C–Cl, pero por la disposición tetraédrica de los mismos el momento dipolar termina anulándose vectorialmente.
Enlaces dativos o de coordinación
Cuando un átomo cede un par de electrones para formar un enlace covalente con otro átomo, se habla entonces de un enlace dativo o de coordinación. Por ejemplo, teniendo B: el par de electrones disponible, y A (o A+), una vacancia electrónica, se forma el enlace B:A.
En la estructura de la vitamina B12 los cinco átomos de nitrógeno se enlazan al centro metálico de Co mediante este tipo de enlace covalente. Estos nitrógenos ceden su par de electrones libres al catión Co3+, coordinándose el metal con ellos (Co3+:N–)
Otro ejemplo puede encontrarse en la protonación de una molécula de amoníaco para formar amonio:
H3N: + H+ => NH4 +
Nótese que en ambos casos es el átomo de nitrógeno quien aporta los electrones; por lo tanto, el enlace covalente dativo o de coordinación ocurre cuando un átomo por sí solo aporta el par de electrones.
Del mismo modo, la molécula de agua puede protonarse para transformarse en el catión hidronio (u oxonio):
H2O + H+ => H3O+
A diferencia del catión amonio, el hidronio todavía tiene un par de electrones libre (H3O:+); sin embargo, es muy difícil que acepte otro protón para formar el inestable dicatión hidronio, H4O2+.
-Enlace iónico

En la imagen se muestra una colina blanca de sal. Las sales se caracterizan por tener estructuras cristalinas, es decir, simétricas y ordenadas; altos puntos de fusión y ebullición, altas conductividades eléctricas al fundirse o disolverse, y también, sus iones se encuentran fuertemente unidos por interacciones electrostáticas.
Estas interacciones conforman lo que se conoce como el enlace iónico. En la segunda imagen se mostró a un catión A+ rodeado de cuatro aniones B–, pero esta es una representación 2D. En tres dimensiones, A+ debería tener otros aniones B– adelante y detrás del plano, formando diversas estructuras.
Así, A+ puede tener seis, ocho, o incluso, doce vecinos. El número de vecinos que rodea un ion en un cristal se conoce como número de coordinación (N.C). Para cada N.C viene asociada un tipo de arreglo cristalino, lo que a su vez constituye una fase sólida de la sal.
Los cristales simétricos y facetados vistos en las sales se deben al equilibrio establecido por las interacciones de atracción (A+ B–) y repulsión (A+ A+, B– B–) electrostáticas.
Formación
Pero, ¿por qué A+ y B–, o Na+ y Cl–, no forman enlaces covalentes Na–Cl? Porque el átomo de cloro es mucho más electronegativo que el metal sodio, el cual además se caracteriza por ceder muy fácilmente sus electrones. Cuando estos elementos se encuentran, reaccionan exotérmicamente para producir la sal de mesa:
2Na(s) + Cl2(g) => 2NaCl(s)
Dos átomos de sodio cede su único electrón de valencia (Na·) a la molécula diatómica de Cl2, para así formar los aniones Cl–.
Las interacciones entre los cationes sodio y los aniones cloruros, aunque representan un enlace más débil que los covalentes, son capaces de mantenerlos fuertemente unidos en el sólido; y este hecho se refleja en el alto punto de fusión de la sal (801ºC).
Enlace metálico

El último de los tipos de enlace químico es el metálico. Este puede encontrarse en cualquier pieza metálica o de aleación. Se caracteriza por ser especial y diferente de los demás, debido a que los electrones no pasan de un átomo a otro, sino que recorren, como un mar, el cristal de los metales.
Así, los átomos metálicos, a decir el cobre, entremezclan sus orbitales de valencia unos con otros para formar bandas de conducción; por las cuales, los electrones (s, p, d o f) transitan entorno a los átomos y los mantiene fuertemente unidos.
Dependiendo del número de electrones que transiten por el cristal metálico, los orbitales aportados para las bandas, y del empaquetamiento de sus átomos, el metal puede ser blando (como los metales alcalinos), duro, brillante, o buen conductor de la electricidad y el calor.
La fuerza que mantiene unidos los átomos de los metales, como los que componen el hombrecillo de la imagen y su portátil, es superior a la de las sales.
Esto puede comprobarse experimentalmente porque los cristales de las sales pueden partirse en varias mitades ante una fuerza mecánica; mientras que una pieza metálica (compuesta de cristales muy pequeños) se deforma.
Ejemplos de enlaces
Los siguientes cuatro compuestos engloban los tipos de enlaces químicos explicados:
-Fluoruro de sodio, NaF (Na+F–): iónico.
-Sodio, Na: metálico.
-Flúor, F2 (F–F): covalente no polar, debido a que hay una ΔE nula entre ambos átomos por ser idénticos.
-Fluoruro de hidrógeno, HF (H–F): covalente polar, ya que en este compuesto el flúor es más electronegativo que el hidrógeno.
Hay compuestos, como la vitamina B12, que posee tanto enlaces covalentes polares como iónicos (en la carga negativa de su grupo fosfato –PO4 ––). En algunas estructuras complejas, como la de los clusters metálicos, pueden incluso coexistir todos estos tipos de enlaces.
La materia ofrece en todas sus manifestaciones ejemplos de enlaces químicos. Desde la piedra en el fondo de un estanque y el agua que la rodea, hasta los sapos que croan en sus bordes.
Si bien los enlaces pueden ser simples, el número y disposición espacial de los átomos en la estructura molecular abren paso a una rica diversidad de compuestos.
Importancia del enlace químico
¿Cuál es la importancia del enlace químico? El incalculable número de consecuencias que desataría la ausencia del enlace químico resalta su enorme importancia en la naturaleza:
-Sin él, no existirían los colores, pues sus electrones no absorberían la radiación electromagnética. Las partículas de polvo y hielo presentes en la atmósfera desaparecerían, y por lo tanto, el color azul del cielo se tornaría oscuro.
-El carbono no podría formar sus interminables cadenas, de las cuales derivan billones de compuestos orgánicos y biológicos.
-Las proteínas no podrían siquiera definirse en sus aminoácidos constituyentes. Los azúcares y las grasas desaparecerían, así como cualquier compuesto carbonado en los organismos vivos.
-La Tierra se quedaría sin atmósfera, porque en ausencia de los enlaces químicos en sus gases, no habría fuerza que los mantuviera unidos. Tampoco habría la más mínima interacción intermolecular entre ellos.
-Las montañas quizás se esfumarían, debido a que sus rocas y minerales, aunque pesados, no podrían contener empaquetados sus átomos dentro de sus estructuras cristalinas o amorfas.
-El mundo estaría formado por átomos solitarios incapaces de formar sustancias sólidas ni líquidas. Esto también traería como consecuencia la desaparición de toda transformación de la materia; es decir, no habría ninguna reacción química. Solo gases fugaces por doquier.
Referencias
- Harry B. Gray. (1965). Electrons and Chemical Bonding. W.A. BENJAMIN, INC. P 36-39.
- Whitten, Davis, Peck & Stanley. Química. (8va ed.). CENGAGE Learning, p 233, 251, 278, 279.
- Nave R. (2016). Chemical Bonding. Recuperado de: hyperphysics.phy-astr.gsu.edu
- Chemical Bond Types. (03 de octubre de 2006). Tomado de: dwb4.unl.edu
- Formation of chemical bonds: The role of electrons. [PDF]. Recuperado de: cod.edu
- CK-12 Foundation. (s.f.). Energy and Covalent Bond Formation. Recuperado de: chem.libretexts.org
- Quimitube. (2012). Enlace covalente coordinado o dativo. Recuperado de: quimitube.com
Cuantos Tipos De Vitamina D Hay
Source: https://www.lifeder.com/enlace-quimico/
